Gastrite atrofica autoimmune
La gastrite atrofica metaplastica autoimmune è una malattia ereditaria autoimmune che colpisce le cellule parietali dello stomaco, causando ridotta secrezione acida e ridotta produzione di fattore intrinseco.
La gastrite cronica atrofica autoimmune (tipo A) rappresenta circa il 10% delle forme di gastrite cronica. Il restante 90% è occupato dalle gastriti croniche atrofiche definite di tipo B e dovute all'infezione cronica da Helicobacter pylori.
I pazienti con gastrite atrofica metaplastica autoimmune hanno auto-anticorpi contro le cellule parietali e i loro componenti (che comprendono il fattore intrinseco e la pompa protonica H+,K+-ATPasi). Ciò determina un accumulo di linfociti a livello dello stomaco con conseguente distruzione della mucosa.
Come conseguenza si ha:
- Riduzione del fattore intrinseco con incapacità ad assorbire vitamina B12
- Ridotta produzione di acido gastrico con aumento della gastrina
E’ ereditata come tratto autosomico dominante ed essendo una malattia autoimmune si associa spesso ad altre patologie autoimmuni come Tiroidite di Hashimoto e la vitiligine.
Si può associare anche a ipoparatiroidismo, m. di Addison, diabete, ipotiroidismo
È inoltre noto come la gastrite atrofica sia direttamente correlata con l'età del paziente, con una prevalenza maggiore degli individui di età superiore ai 70 anni, benché siano riportanti casi anche in soggetti di età inferiore ai 40 anni.
In alcuni pazienti, coesiste una infezione cronica da Helicobacter pylori, anche se la relazione non è chiara.
Le aree di gastrite atrofica nel corpo e nel fondo possono presentare la sostituzione di cellule gastriche con cellule di tipo intestinale (metaplasia).
Sintomi
I sintomi sono correlati soprattutto al Deficit Vit B12 :
- anemia macrocitica (astenia, tachicardia, pallore)
- disturbi intestinali (stipsi da distruzione mielinica)
- disturbi neurologici (parestesie, disturbi della sensibilità tattile propriocettiva, paresi, atassia, riflessi patologici, demenza )
La presenza di tutti e tre i disturbi configura la Triade di Biemer.
Ma non sempre i pazienti manifestano i disturbi elencati, anzi, il più delle volte è possibile che la malattia decorra in modo asintomatico per lungo tempo, o al limite causi sintomi aspecifici sia di tipo intestinale (difficoltà digestive, diarrea, calo dell’appetito, malassorbimento, perdita di peso, glossite) che neurologico (sensazione di intorpidimento di mani/piedi, disturbi della sensibilità, amnesia).
Complicazioni
I pazienti con gastrite atrofica hanno un rischio 3 volte superiore di sviluppare il cancro allo stomaco.
Secondo quanto confermato da numerosi studi esiste un modello di progressione ben preciso, noto come cascata di Correa, per cui una mucosa gastrica normale può trasformarsi in cancro.
In un arco di tempo, più o meno lungo, possiamo osservare:
- Alterazioni rigenerative, ovvero un'iperplasia reattiva al danno subito.
- Metaplasia, caratterizzata da sostituzione dell'epitelio gastrico da parte di epitelio con caratteristiche tipicamente intestinali (metaplasia intestinale).
- Atrofia, reperto tipico e importante caratterizzato da perdita progressiva delle cellule parietali e delle ghiandole corpo-fundiche. Tipica della forma autoimmune è un'intensa iperplasia (per ridotta acidità del lume gastrico) delle cellule G confinate nella mucosa dell'antro gastrico, che producono gastrina.
- Displasia, da non confondere con quadri di intensa iperplasia reattiva. Di solito la displasia insorge a livello dell'epitelio metaplastico; le cellule presentano forme mitotiche atipiche, dimensioni notevoli e orientamento anomalo. La displasia è considerata una condizione precancerosa, in quanto spesso associata allo sviluppo di carcinoma in situ.
- e infine cancro
Queste tappe sono sequenziali ed obbligate. Di qui la necessità di un attento follow-up,
In alcuni casi l’iperplasia delle cellule enterocromaffino-simili legata agli elevati livelli di gastrina progredisce fino a tumore carcinoide.
Diagnosi
Il sospetto di gastrite autoimmune viene in presenza di una anemia macrocitica con associati bassi livelli di vit. B12 e acido folico, presenza di anticorpi anti cellule parietali (PCA), anti fattore intrinseco (IFA), anti-perossidasi (TPO), alti livelli di gastrina.
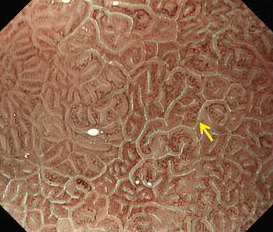
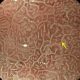
figura 1: metaplasia intestinale
La conferma della diagnosi la si ha solo con la esofago gastroscopia ed un protocollo bioptico completo: 2 biopsie all’antro, 1 all’angulus, 2 al corpo, 2 al fondo e in tutte le sedi sospette. Per questo l’esame deve essere fatto con endoscopio ad alta definizione con filtraggio NBI o simile della luce. Migliori risultati diagnostici si li abbiamo avuti con l’endoscopia ad autofluorescenza, ma questo è uno strumento a disposizione di pochi centri in Europa.

Figura 2: diagnostica in autofluorescenza
Con l’endoscopia oltre che la diagnosi possiamo fare una corretta stadiazione della malattia in base alla quale stabilire un corretto follow-up.
Trattamento
Non esiste una terapia causale in grado di bloccare la malattia. In alcuni casi, gli immunosoppressori ed i corticosteroidi possono essere utilizzati per rallentarne lo sviluppo.
Nei pazienti che sviluppano anemia perniciosa è necessario il supplemento parenterale o per os di cianocobalamina (vitamina B12) che in piccole dosi viene assorbita anche in assenza di fattore intrinseco.
In alcuni casi può essere utile il trattamento dell’ipocloridria con la somministrazione per via orale, durante i pasti, di acido cloridrico diluito per lo più in associazione con pepsina.
Non è indicato, anzi è sconsigliato, abbassare il pH del succo gastrico con un antiacido o un inibitore della pompa protonica, in quanto è presenta ipocloridria e non iperacidità.
Possono essere indicati invece protettori della mucosa gastrica perché l’ipergastrinemia determina un rilasciamento del piloro e reflusso duodeno-gastrico di bile.
Sorveglianza
Con frequenza variabile a seconda della gravità della malattia e dei sintomi dovrà essere controllato l'emocromo, la Vit. B12 , i folati, la sideremia e la ferritina per le necessarie integrazioni. Ma i pazienti devono essere soprattutto monitorati tramite esecuzione di esofagogastroduodenoscopie a cadenza regolare (ogni 3 anni) onde valutare lo stato dell'infiammazione ed attuare una diagnosi precoce per un eventuale sviluppo di un linfoma o di un carcinoma gastrico che, come abbiamo detto, ha una incidenza 3 volte superiore alla popolazione normale.
|
Score Atrofia |
CORPO |
||||
|
No Atrofia (score 0) |
Atrofia lieve |
Atrofia moderata |
Atrofia severa |
||
|
ANTRO-ANGULUS |
No Atrofia (score 0) |
Stadio 0 |
Stadio 1 |
Stadio 2 |
Stadio 2 |
|
Atrofia lieve (score 1) |
Stadio1 |
Stadio 1 |
Stadio 2 |
Stadio 3 |
|
|
Atrofia moderata (score 2) |
Stadio 2 |
Stadio 2 |
Stadio 3 |
Stadio 4 |
|
|
Atrofia severa (score 3) |
Stadio 3 |
Stadio 3 |
Stadio 4 |
Stadio 4 |
|
Figura 3 classificazione OLGA (Operative Link on Gastritis Assessment – OLGA)
Protocollo di follow-up
I controlli dovranno essere più ravvicinati con diagnosi bioptica di displasia.
Ugualmente indicato il controllo nei pazienti con familiarità per gastrite autoimmune, ma le linee guida non sono concordi nel timing.
Gastrite atrofica |
|
Atrofica auto-immune |
||
|
Stadio 0 -1 |
Non FU |
|
Ogni 3 anni | |
| Stadio 2 | Ogni 3 anni | Displasia | Ogni 2 anni | |
| Stadio 3-4 | Ogni 2 anni |
Familiarità per G.A.AI |
Ogni 3-5anni |
|
Guideline: Management of epithelial precancerous conditions and lesions in the stomach (MAPS II): European Society of Gastrointestinal Endoscopy (ESGE), European Helicobacterand Microbiota Study Group (EHMSG), European Society of Pathology (ESP), and Sociedade Portuguesa de Endoscopia Digestiva (SPED) guideline update 2019
Forum di pazienti con gastrite atrofica autoimmune: www.gcaa.altervista.org